利用双光学梳成功实现光学生物传感:高灵敏度和快速检测生物分子
发布时间:2023-09-27 10:09:40 阅读数: 217

图 1. 使用 OFC 进行基于电频读出的光学生物传感。资料来源:德岛大学
生物传感器是一种生物分子传感器,利用或模仿生物体复杂的分子识别能力。它们广泛应用于医疗保健、食品和环境等领域。
特别是光学生物传感器,它通过光学方式读取目标分子与分子识别元件之间的相互作用,具有高精度和快速测量的能力。然而,事实证明它们在超早期检测新型冠状病毒(SARS-CoV-2)和癌细胞方面的灵敏度不够。
由德岛大学后 LED 光子学研究所的 Takeshi Yasui 教授和客座副教授 Taira Kajisa、德岛大学先进技术与科学研究生院的博士课程学生 Shogo Miyamura 和高知工科大学系统工程学院的 Shuji Taue 副教授组成的研究小组将作为下一代激光器而备受关注的光频率梳 (OFC) 不是用作光源,而是用作生物传感的传感器。他们的研究成果发表在《科学报告》上。
在这项研究中,研究小组利用 OFC 独特的光电频率转换特性解决了上述难题,实现了光频域传感和电频域读出。此外,通过采用双 OFC(双 OFC)并实施主动假温度补偿,研究人员缓解了生物传感中常见的温度漂移问题。
这一突破实现了对 SARS-CoV-2 的快速和高灵敏度检测,为超早期检测新出现和再次出现的传染性病毒以及包括癌症和环境污染物在内的健康生物标志物带来了希望。
研究背景和历史
生物传感器能够检测各种天然生物分子,如糖、核酸和蛋白质,利用或模仿生物体复杂的分子识别功能。这些生物分子传感器可广泛应用于医疗保健、食品和环境等领域。尤其是光学生物传感器,它能以光学方式读取目标分子与分子识别元件之间的相互作用,具有高灵敏度、高精度和快速测量等特点。
然而,目前仍需要进一步提高灵敏度。人们相信,大幅提高光学生物传感器的灵敏度可以实现对新型冠状病毒(SARS-CoV-2)和癌症的超早期检测。要大幅提高灵敏度,就必须采用一种根本不同的技术方法。
在光学生物传感技术中,测量是基于依赖于样品浓度的光谱偏移。然而,与光学光谱的宽度相比,这种偏移相对较小,因此光学光谱测量设备的性能限制制约了生物传感的灵敏度。
如果有可能将依赖于样品浓度的光学频谱偏移转换成相应的电学频谱偏移进行测量,那么就可以在光学领域实现高灵敏度,同时提供易于处理和高精度的电信号测量。
因此,研究小组将目光转向了光频梳(OFC),将其作为将光学频谱偏移转换为电学频谱偏移的一种手段。
他们说,通过利用 OFC,我们可以将 1014 Hz 的光频率信号精确地转换成 108 Hz 的电频率信号,从而可以利用高性能、高性价比的电频率测量设备来进行基于电频率信号读出的光学生物传感。因此,我们正在开展以 OFC 为核心技术的生物传感研究,我们相信这项技术在提高生物传感能力方面大有可为。
研究内容和成果
OFC 具有高度离散的多光谱结构,其中许多光频模式(OFC 模式)像梳齿一样均匀分布(图 1,上半部分)。每个 OFC 模式的光频 νm 可用下式表示:
νm=fceo+mfrep
其中,fceo 表示载波包络偏移频率,frep 表示模式间距,m 表示模式阶数。νm 是 1014 Hz 的光频率信号,而 frep 和 fceo 则是 108 Hz 的电频率信号。这个等式表示通过 OFC 连接光频率信号和电频率信号。
例如,通过激光控制将 frep 和 fceo 与电频率标准锁相,可将电频率标准的不确定性转移到 νm,从而使 OFC 成为由电频率标准保证的 "光学频率标尺"(图 1,左下方)。
反过来,也可以利用这种关系将光频信号转换为电频信号。例如,将光纤生物传感器置于光纤 OFC 的谐振器中,可将与样品浓度相关的光频谱偏移(νm 偏移)转换为电频谱偏移(frep 偏移)(图 1,右下方)。
电频率信号得益于高精度国家标准和高性能、高性价比测量设备的存在,从而实现了高精度、宽动态范围、快速和便捷的测量。
利用 "OFC 中的光电频率转换 "和 "高精度电频率测量 "之间的良好协同作用,我们成功实现了基于电频率读出的光学生物传感(生物传感 OFC)。这种新方法将光学频率域的高灵敏度与电频率读数的易操作性和精确性结合在一起。
光纤 OFC 的光谐振器长度的倒数决定了 frep 的温度漂移,而环境温度的变化会导致光谐振器长度的热胀冷缩,从而使 frep 发生变化。
这种由温度引起的自由度变化在传感器信号上叠加为温度漂移。由于温度漂移引起的自由频谱变化往往大于样品浓度变化引起的自由频谱偏移,因此采用了主动假温度补偿方法(图 2)。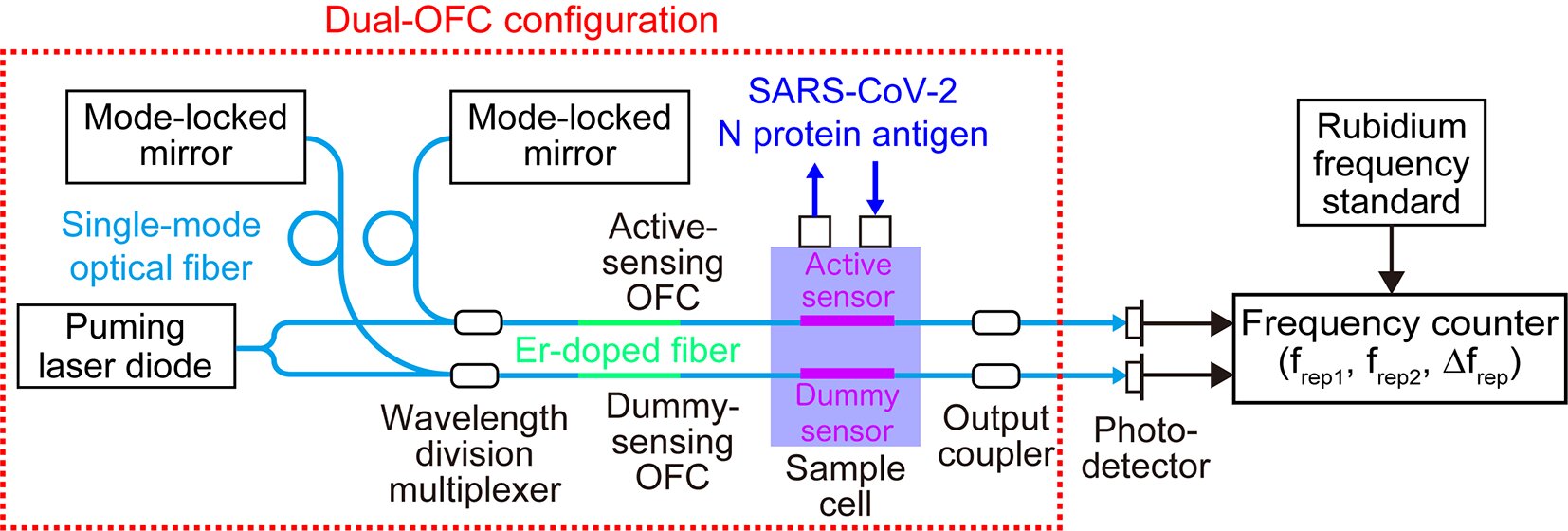
图 2. 利用双 OFC 的有源假温度补偿。资料来源:德岛大学
在这种方法中,等效光纤 OFC 谐振器成对制备(双 OFC)。其中一个空腔(主动传感 OFC,模式间距 = frep1)包含一个经过表面改装的光纤传感器,用于生物传感(主动传感器),而另一个空腔(模拟传感 OFC,模式间距 = frep2)仍然是另一个没有表面改装的光纤传感器(模拟传感器)。由于两个传感器都放置在同一个样品池中,只有有源传感器对抗原敏感,而温度漂移对两个传感器的影响相似。
因此,通过测量主动传感 OFC 和虚拟传感 OFC 之间的差分信号(Δfrep = frep1-frep2),可以补偿温度漂移的影响,并只提取与样品浓度相关的信号。这种创新方法大大提高了生物传感 OFC 的准确性和可靠性,在减轻温度波动影响的同时,实现了对生物分子的精确和实时检测。
在本实验中,我们一边测量,一边以 10 分钟为间隔逐步改变磷酸盐缓冲盐水(PBS)中 SARS-CoV-2 核苷酸(N)蛋白抗原的浓度。

图 3. 实验结果。资料来源:德岛大学
图 3(a)显示了主动传感 OFC 和模拟传感 OFC 的传感器信号(frep1 和 frep2)的变化。在这两个传感器信号中,都观察到了温度漂移引起的渐变,但在主动传感 OFC 信号中,没有证据表明与抗原浓度有关的阶跃变化。这是因为温度引起的 frep 变化比抗原浓度变化引起的 frep 移动更为显著。
图 3(b)显示了两个传感器之间提取的差分信号(Δfrep)。温度漂移被有效抑制,与抗原浓度相对应的阶跃变化清晰可见。根据测量结果,我们绘制了抗原摩尔浓度与传感器信号之间的关系图,如图 3(c)中的红圈图所示。
为了评估实验结果的有效性,我们使用理论模型(紫色线)进行了曲线拟合分析。分析结果证实,在 10 分钟的测量时间内,摩尔浓度的检测限为 37aM。这一严格的验证强调了我们的生物传感方法的准确性和可靠性,以及它在检测极低浓度 SARS-CoV-2 N 蛋白抗原方面的卓越灵敏度。

图 A.资料来源:德岛大学
未来发展
虽然这项测量是在理想条件下进行的,PBS 中只有 SARS-CoV-2 蛋白抗原,但由于非特异性吸附,实际样品(如唾液、鼻咽拭子和鼻拭子)中往往含有大量不需要的蛋白质(干扰物质)。这种非特异性吸附会限制灵敏度和精确度。
在今后的工作中,我们计划考虑实际样品,并采用传感器表面改性方法来防止非特异性吸附。这将使我们能够在与实际情况非常相似的条件下评估性能,并确保我们的生物传感技术在实际应用中的准确性和可靠性。
参考资料
Shogo Miyamura et al, Rapid, high-sensitivity detection of biomolecules using dual-comb biosensing, Scientific Reports (2023). DOI: 10.1038/s41598-023-41436-3